Na série de artigos sobre Processamento Digital de Sinais (PDS) no blog Insights apresentamos inicialmente uma visão panorâmica desta área de competência da CERTI e, posteriormente, focalizamos mais especificamente as aplicações em agricultura digital. No primeiro artigo já havíamos mencionado o papel importante que o PDS exerce na área da saúde digital e agora vamos explorar mais detalhadamente as aplicações biomédicas desta tecnologia.
Para começar, um pouco de história!
Considera-se que o primeiro cientista a medir uma corrente bioelétrica foi o italiano Carlo Matteucci, que em 1838 registrou correntes geradas por contrações musculares. Outros pioneiros dos experimentos em bioeletromagnetismo foram o fisiologista alemão Emil du Bois-Reymond, que em 1842 conseguiu detectar a passagem de corrente elétrica em nervos, o neurofisiologista inglês Richard Caton, que em 1875 registrou tensões geradas pela atividade cerebral, e o pesquisador também inglês Augustus Waller, que em 1887 usou eletrodos afixados ao peito para registrar as tensões geradas pela atividade cardíaca. Embora não seja baseada em bioeletromagnetismo, a descoberta dos raios X em 1895 pelo físico e engenheiro mecânico alemão Wilhelm Röntgen é outro importante marco dos primórdios da tecnologia médica moderna. Estas descobertas científicas levaram posteriormente ao desenvolvimento dos primeiros equipamentos eletromédicos analógicos para auxílio ao diagnóstico: apenas um ano após a descoberta de Röntgen as empresas Siemens e General Electric já comercializavam aparelhos de raios X; em seguida foram apresentados o eletrocardiógrafo em 1903 pelo pesquisador holandês Willem Einthoven, o eletroencefalógrafo em 1924 pelo psiquiatra alemão Hans Berger e o eletromiógrafo em 1942 pelo canadense Herbert Jasper. Mais tarde, já na década de 1960, surgiram os primeiros equipamentos de ultrassonografia analógica, capazes de formar imagens a partir dos ecos gerados pelas variações de impedância acústica em estruturas anatômicas internas.
A digitalização dos equipamentos eletromédicos
O processamento digital de sinais biomédicos teve início quando os computadores tornaram-se mais disponíveis para a comunidade científica após a Segunda Guerra Mundial. No final dos anos 50 pesquisadores da George Washington University e do Massachusetts Institute of Technology (MIT) publicaram os primeiros algoritmos para análise de eletrocardiogramas e eletroencefalogramas, respectivamente. Também naquela época imagens médicas começaram a ser digitalizadas e processadas por computador para análise morfológica celular e para contagem automática de culturas bacterianas. Em linhas gerais, o processamento de sinais e imagens biomédicos consiste na aplicação de algoritmos, principalmente para execução de operações matemáticas, a dados biológicos e médicos, em geral coletados de um paciente por meio de sensores. Tipicamente, os dados são primeiro submetidos a operações de pré-processamento, tais como a filtragem digital para redução do nível de ruído, e em seguida, são aplicados algoritmos para extração de parâmetros relevantes para o diagnóstico médico. No caso de eletrocardiogramas, por exemplo, os parâmetros podem ser os intervalos temporais entre determinados pontos da forma de onda, a dimensão fractal do sinal ou a energia dos coeficientes de wavelets em uma determinada escala. O último passo é a identificação de padrões e/ou a classificação das medições dos parâmetros em classes que correspondem a condições consideradas normais e anormais. Usando novamente o caso dos eletrocardiogramas, as classes de condições anormais podem corresponder a infarto do miocárdio, taquicardia, extrassístole e outras arritmias, por exemplo.
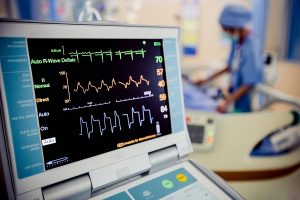
Na década de 1970, os processadores embarcados viabilizaram o surgimento de versões digitais dos equipamentos eletromédicos analógicos desenvolvidos na primeira metade do século, realizando em tempo real muitas das análises que anteriormente só eram possíveis mediante o pós-processamento dos sinais em computadores de grande porte, e armazenando os dados coletados de forma mais eficiente e prática do que nos antigos gráficos em rolos de papel. Além dos eletrocardiógrafos, eletroencefalógrafos e eletromiógrafos, vários outros equipamentos eletromédicos digitais derivados de antecessores analógicos fazem amplo uso de PDS, como os esfignomanômetros (para medição da pressão arterial), oxímetros (concentração de oxigênio no sangue), fotopletismógrafos (ritmo cardíaco, por meios ópticos), eletrooculógrafos (movimentos oculares), eletroretinógrafos (resposta da retina a estímulos luminosos) e espirômetros (capacidade pulmonar). Há também os monitores de parâmetros vitais, que combinam as funções de dois ou mais destes aparelhos. O PDS também desempenha um papel fundamental na tecnologia médica assistiva, como nos aparelhos auditivos digitais, implantes cocleares, sintetizadores de voz e outros.
A revolução da imagiologia médica digital
Atualmente, equipamentos para o diagnóstico assistido por imagens são uma das principais aplicações do PDS na área da saúde. Dentre estes, os aparelhos de radiografia digital e os de ultrassonografia digital derivam de precursores analógicos, tendo porém desempenho muito superior. Vários outros aparelhos, no entanto, não possuem antecessores analógicos, tendo surgido apenas graças ao advento do PDS, que pode ser considerado, portanto, sua tecnologia viabilizadora. Como mencionado no primeiro artigo desta série, o princípio comum a vários destes equipamentos é o de usar as informações parciais contidas em sinais uni- ou bidimensionais para compor sinais de dimensões superiores, tendo por base uma técnica denominada tomografia computadorizada e outras dela derivadas. O nome vem do grego tomos + graphō = desenho de seção, pois tipicamente o resultado do processamento é uma imagem representando a densidade dos tecidos ou outra propriedade fisiológica de uma seção planar do corpo do paciente, sem a superposição de imagens que ocorre na radiografia convencional. Desenvolvida inicialmente nas décadas de 1960 e 1970, esta tecnologia provocou uma verdadeira revolução na imagiologia médica. Dentre os pesquisadores responsáveis pelo seu desenvolvimento destacam-se Allan Cormack e Godfrey Hounsfeld, cujo trabalho pioneiro foi reconhecido com o Prêmio Nobel de Medicina de 1979.
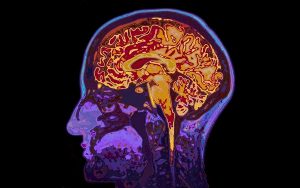
Na tomografia computadorizada (também chamada de tomografia computadorizada axial) a imagem é formada a partir de sinais de raios X captados por sensores unidimensionais dispostos em volta do corpo do paciente. Uma tecnologia semelhante é utilizada nos aparelhos de ressonância magnética (conhecida pela sigla MRI, do inglês magnetic resonance imaging), que utilizam campos magnéticos e ondas de rádio em lugar dos raios X, evitando a exposição do paciente à radiação ionizante e seus possíveis efeitos nocivos. Embora a ressonância magnética seja, em geral, preferível, a tomografia computadorizada é mais indicada para determinados tipos de exames e continua sendo usada hoje em dia. Outras tecnologias derivadas da tomografia computadorizada são a tomografia por emissão de pósitrons (conhecida pela sigla PET, do inglês positron emission tomography), usada para observar processos metabólicos corporais, a ressonância magnética de difusão, usada para obter informações do sistema nervoso, tais como modelos tridimensionais das conexões neurais no cérebro, a tomografia óptica, a ressonância magnética funcional, a angiotomografia e outras.
Levando o laboratório até o paciente
O processamento digital de sinais e imagens também é uma tecnologia-chave para o desenvolvimento de aparelhos eletromédicos que permitem fazer análises clínicas de forma rápida e descentralizada. São aparelhos feitos para realização de testes in vitro no ponto de atendimento ao paciente (em inglês, point of care), tais como consultórios médicos, postos de saúde, ou mesmo em ambulâncias, residências ou locais atendidos por agentes comunitários de saúde. Evita-se, assim, que o paciente tenha que deslocar-se até um laboratório de análises clínicas ou que amostras biológicas coletadas devam ser enviadas a um laboratório para a realização do exame. Isto traz inegáveis benefícios: o médico pode completar o diagnóstico e prescrever o tratamento durante a consulta; o agente comunitário de saúde pode realizar prontamente a triagem e o encaminhamento de pacientes para tratamento; em certos casos, o próprio paciente pode controlar de forma mais precisa seu tratamento, como acontece, por exemplo, com diabéticos que utilizam testes para medição do nível de glicose no sangue. Estes aparelhos podem ser muito úteis até no ambiente hospitalar, onde, mesmo havendo a disponibilidade de um laboratório de análises clínicas, a obtenção mais rápida do resultado na própria UTI ou sala de emergência pode ser decisiva em situações críticas, como, por exemplo, no tratamento da sepse, em que a probabilidade de sobrevivência do paciente diminui a cada hora de demora na identificação dos agentes infecciosos.
Recentemente, a conhecida Fundação XPRIZE realizou uma competição tecnológica para o desenvolvimento experimental de um aparelho portátil para diagnóstico de 12 doenças e aquisição de cinco sinais vitais em tempo real, denominado Tricorder (em alusão a um aparelho usado em uma série televisiva de ficção científica). A importância do desenvolvimento de aparelhos para diagnóstico no ponto de atendimento é atestada por sua escolha como objeto desta competição da Fundação XPRIZE, cujos outros desafios recentes incluem o envio de uma sonda espacial à lua por uma entidade privada e a redução do tempo e custo necessários para a realização do sequenciamento do genoma humano.
Como exemplo desta aplicação do PDS podemos citar o projeto PodiTrodi (Technology Platform for Point of Care Diagnostics for Tropical Diseases), no qual um consórcio de 13 instituições brasileiras e europeias, entre elas a Fundação CERTI, o CTI, a Unicamp, a Fundação Oswaldo Cruz (Fiocruz)/Insituto de Biologia Molecular do Paraná (IBMP) e o Instituto Fraunhofer ENAS, desenvolveram o protótipo de um aparelho para diagnóstico da doença de Chagas no ponto de atendimento. O aparelho realiza um imunoensaio combinado com um teste de ácidos nucleicos por reação em cadeia da polimerase (em inglês polymerase chain reaction — PCR) em um cartucho microfluídico descartável, de forma a detectar a presença do parasita Trypanosoma cruzi tanto na fase de infecção aguda inicial quanto na fase crônica da doença.[1] Um sistema de visão computacional embarcado captura e analisa imagens das câmaras reagentes do cartucho, fornecendo automaticamente o resultado do teste. Outro exemplo de projeto nesta área é a cooperação entre CERTI, UFSC, MIT e Fiocruz/IBMP para desenvolvimento de uma plataforma de microscopia embarcada baseada em holografia digital em linha.[2] Por não necessitar de lentes, esta plataforma é robusta, leve e compacta, o que a torna particularmente atraente para o uso em aparelhos portáteis para diagnóstico no ponto de atendimento.
Para Saber Mais
Cobra, D. T. e Costa, A. D. T., Tecnologia para diagnóstico no ponto de atendimento. Revista Polyteck, nº 14, outubro de 2015, pp. 3-6.
Najarian, K. e Splinter, R., Biomedical Signal and Image Processing, 2nd Ed. CRC Press, Boca Raton, FL, USA, 2012.
Nebeker, F., Golden Accomplishments in Biomedical Engineering. IEEE Engineering in Medicine and Biology Magazine, Vol. 21, No. 3, pp. 17-47, May-Jun 2002.
Sobieranski, A. C. et al., Portable Lensless Wide-field Microscopy Imaging based on Digital In-line Holography and Multi-Frame Pixel Super-Resolution, Light: Science & Applications, Vol. 4, e346, Oct. 2015.
[1] Processo CNPq Nº 590.032/2011-9 e FP7 Nº 287.770
[2] Processo CNPq Nº 551.967/2011-0







